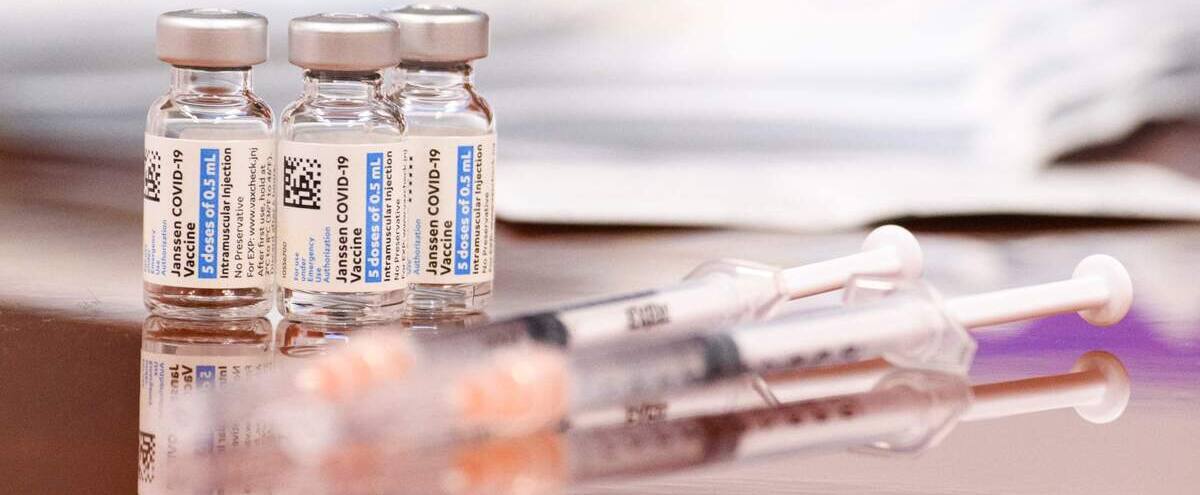
Johnson & Johnson demande l’autorisation pour une dose de rappel de son vaccin anti-COVID
Le Journal de Montréal
WASHINGTON | Le groupe pharmaceutique Johnson & Johnson a annoncé mardi avoir soumis des données à l’Agence américaine des médicaments (FDA) en vue d’obtenir l’autorisation pour une injection de rappel chez les adultes de son vaccin unidose contre la COVID-19.
• À lire aussi: Le vaccin Pfizer efficace contre les formes graves au moins 6 mois, selon une étude
• À lire aussi: COVID-19: l’Espagne élargit la troisième dose aux plus de 70 ans
• À lire aussi: Le régulateur européen approuve une troisième dose du vaccin Pfizer pour les plus de 18 ans
Ces données incluent les résultats d’une étude clinique selon laquelle une deuxième dose injectée environ deux mois (56 jours) après la première montre une efficacité de 94 % contre les cas symptomatiques (modérés à graves) aux États-Unis, et de 100 % contre les cas graves 14 jours après cette seconde injection, a rappelé l’entreprise dans un communiqué.
Une seconde dose injectée six mois après la première multiplie également « par neuf » les niveaux d’anticorps observés, selon une autre étude de « J&J », et « par douze » quatre semaines après le rappel.
Le vaccin, pris en unidose ou en dose de rappel, est généralement bien toléré par les patients, a assuré le groupe américain.
La FDA a de son côté indiqué que son comité d’experts se réunirait les 14 et 15 octobre pour étudier les demandes d’autorisation de Johnson & Johnson et de la société Moderna.
« Nous attendons avec impatience de discuter avec la FDA et d’autres autorités de santé pour soutenir leurs décisions concernant les doses de rappel », a déclaré Mathai Mammen, responsable recherche et développement chez Janssen, la filiale pharmaceutique de Johnson & Johnson.

